에이프로젠(대표이사 이승호)은 삼중음성유방암 치료제 AP401의 동물모델에 대한 비임상 효능입증 시험을 완료하고 6월내로 글로벌 CDMO업체들 중 한 곳과 생산공정 개발 및 임상시료 생산을 위탁(CDMO)하기 위한 계약 협의가 진행 중이라고 8일 밝혔다.
이번 계약을 통해 에이프로젠은 AP401 임상시료의 생산 일정을 확정하고 추후 상업용 의약품 생산을 위한 기반을 마련하게 되며 글로벌 임상시험을 속도감 있게 진행할 것으로 기대하고 있다. AP401은 글로벌시장을 타깃해 한국을 비롯한 미국, 일본, 호주 등 주요 9개 국가에서 이미 특허 등록을 마쳤고 그 외 9개국에서 특허 심사 중이다.
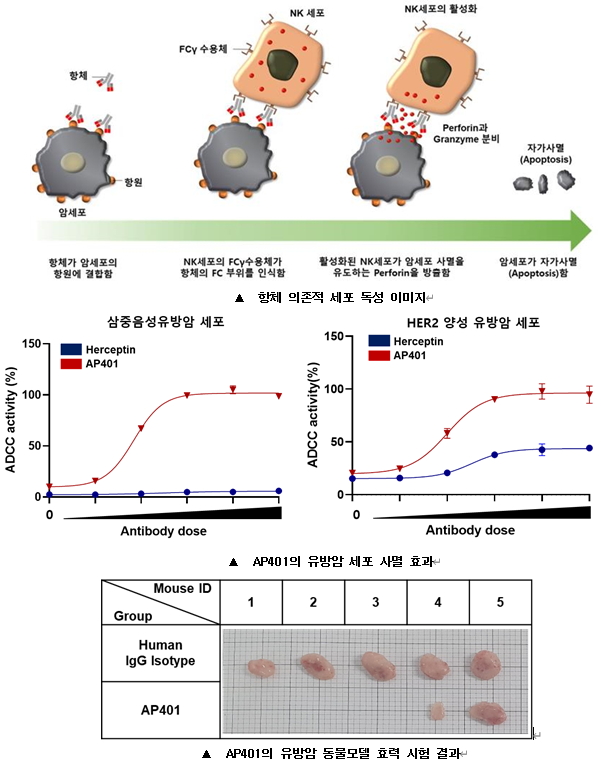
AP401은 삼중음성유방암을 포함하는 유방암에 특이적인 항원을 인식하는 항체 기반 약물로 삼중음성유방암 환자의 115개 암조직 샘플을 분석한 결과 92개의(발현 비율: 80%) 샘플에서 이 항원이 높은 수준으로 발현됨을 확인하였다. 이 항체 약물은 서열 변경을 통해 항체에 의존적으로 암세포를 사멸시키는 기능(ADCC; Antibody-dependent cellular cytotoxicity)을 크게 강화한 약물로 Herceptin®이 1차 치료제로 사용되는 HER2 양성 유방암 및 Herceptin®이 효과를 보이지 않는 삼중음성유방암에서 Herceptin®에 비해 월등한 암세포 사멸 능력을 확인했으며 유방암 동물모델의 60%이상에서 암이 완전 관해(complete response)될 정도로 뛰어난 효과를 확인했다.
에이프로젠 관계자는 “삼중음성유방암은 전체 유방암의 15%를 차지하고 전이가 잘 일어나는 가장 악성인 암종임에도 불구하고 아직까지도 효과적인 표적치료제가 개발되지 못해 여전히 고전적 화학요법에 의존할 수밖에 없어 부작용이 심하고 치료 예후가 좋지 않다”며 “AP401이 동물에서 탁월한 효과가 확인된 만큼 임상에서 효과가 증명된다면 삼중음성유방암 치료제 시장의 게임 체인저가 될 뿐 아니라 효과적인 치료제를 간절히 기다리는 환자에게 새로운 희망이 될 것”이라고 말했다. 또한 “치료제가 시급한 삼중음성유방암을 대상으로 안전성이 확인되면 다른 유방암으로도 적응증을 확대해 나갈 계획”이라고 덧붙였다.
에이프로젠은 AP401을 비롯해 전 제품을 자체 개발한다는 내부 방침이 있었으나 현재 진행 중인 바이오시밀러 4 품목 및 다른 신약 개발 일정에 영향을 주지 않으면서 AP401 프로젝트의 동시 진행을 위해 국내외 글로벌 CDMO 업체들과 협의중에 있다. AP401 세포주는 에이프로젠만의 독자적인 발현 벡터 및 고발현 세포주 제작 기술로 개발 완료됐고 CDMO 기업을 통해 배지 선별 과정부터 임상 1/2a상 시료 생산 단계까지 빠르게 진행될 계획이다.
이 회사는 AP401뿐만 아니라 혈액암 이중항체 치료제, 면역항암제, 골관절염 치료제 등 보유한 다양한 신약파이프라인들이 순차적으로 임상개발 단계 진입도 준비하고 있다. 에이프로젠은 에이프로젠메디신(에이프로젠 MED [007460])과 사업 시너지, 외형 확대를 통한 재무 구조 개선, 경영 효율성 제고 및 자금 조달 역량 강화 등을 위해 합병을 추진하고 있으며 합병 기일은 오는 7월 15일이다.