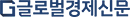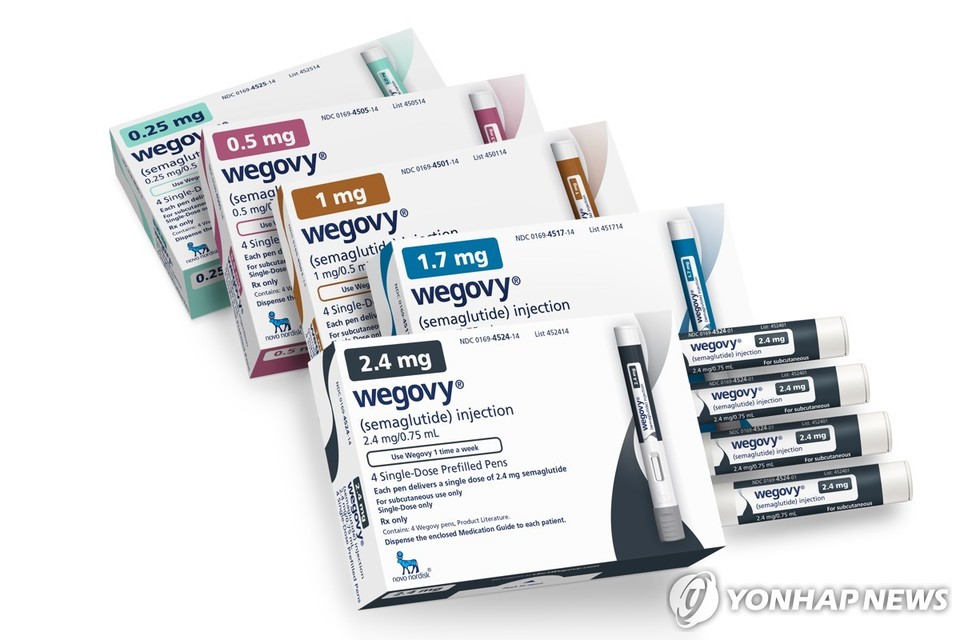
미국 식품의약국(FDA)은 8일(현지시간) 비만 또는 과체중의 심혈관 질환이 있는 성인의 심혈관 관련 사망, 심장마비 및 뇌졸중 위험을 줄이기 위해 비만치료제 '위고비(세마글루타이드)' 주사제의 새로운 적응증을 승인했다.
당뇨병 및 지질장애 부문 책임자인 존 샤렛츠(John Sharretts) 박사는 “위고비는 현재 심혈관 질환이 있고 미국 성인의 약 70%에게 영향을 미치는 비만 또는 과체중이 있는 성인의 생명을 위협하는 심혈관 질환으로 인한 사고을 예방하는 데 도움이 되도록 승인된 최초의 비만치료제이다”라고 말했다
FDA는 “심혈관 질환이 있거나 비만·과체중인 환자 집단이 심혈관으로 인한 사망과 심장마비, 뇌졸중을 겪을 위험이 더 높다"며 "이러한 심혈관 위험을 낮추는 것으로 입증된 치료 선택권을 제공하는 것은 공중 보건의 주요한 발전이다"라고 덧붙였다.
이번 승인은 1만7600여명을 대상으로 진행한 임상시험 결과를 토대로 이뤄졌다. 해당 임상시험은 위고비를 투여한 집단과 위약 투여 집단으로 나눠 진행됐다.
두 집단 모두 혈압·콜레스테롤 관리를 위한 치료와 식이·운동 상담 등을 똑같이 받았으나 심혈관 관련 사망이나 심장마비, 뇌졸중 환자 발생 비율은 위고비 투여 집단이 6.5%로 위약 투여 집단(8.0%)보다 낮았다.
덴마크 제약사 노보노디스크가 생산하는 위고비는 2021년 비만 치료제로 FDA의 승인을 받았다. 당초 2형 당뇨 치료제로 개발됐다가 체중감량 효과가 뛰어나다는 사실이 확인되면서 전 세계적으로 인기를 얻고 있다.
위고비의 성분인 세마글루티드는 글루카곤 유사 펩티드-1(GLP-1) 수용체 작용제로, 포만감을 느끼게 하는 호르몬인 GLP-1과 비슷한 효과를 내 주기적으로 주사하면 체중의 15%가량을 줄이는 데 도움이 되는 것으로 나타났다.